The Hero
الأســــــــــــــطورة

- إنضم
- Jun 29, 2008
- المشاركات
- 20,103
- مستوى التفاعل
- 69
- المطرح
- في ضحكة عيون حبيبي
في الكيمياء تعنى كلمة العطرية أو الأروماتية, هي خاصية كيميائية يكون بها الجزيء له حلقة بها روابط غير مشبعة مترافقة, أو أزوج وحيدة, أو مدارات فارغة لها ثبات أقوى من المتوقع حدوثه من الإقتران بمفرده.
وهذا يقال أنه يحدث بسبب حرية دوران الإلكترونات حول ترتيب دائرى من الذرات, وتتبادل فيما بينها الوضع الأحادي والثنائي للرابطة التساهمية. (لتوضيح أكثر, هذه الروابط يمكن أن تلاحظ كتهجين بين الروابط الأحادية والثنائية, فكل رابطة في الحلقة تكون متطابقة مع الأخرى.) وهذا هو التصور العام للحلقات العطرية الذي تم اقتراحه بواسطة كيكولي. ويتكون هذا التصور للبنزين من شكلان بهما رنين, وهما يمثلان تبادل الوضع للوابط الأحادية والثنائية. ويكون البنزين أكثر ثباتا من "الهيكسا ترايين الحلقي", وهو جزيء نظري.
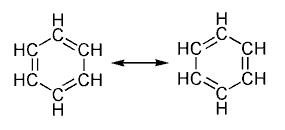
ويمثل السهم ذو الرأسين هنا عملية الرنين. وهندسيا فإن البنزين شكل سداسي تام. وبصفة عامة فإن الرابطة C=C أقصر من C-C, ولا يجب أن يخلط بين الشكلين حيث أن طول الرابطة C-C يتذبذب.
ويوجد تمثيل أفضل لحلقة البنزين, وهو وضع دائرة حيث تتوزع الكثافة الإلكترونية من الرابطة باي أسفل وأعلى الحلقة. وهذا التمثيل للحلقة أفضل في تمثيل الكثافة الإلكترونية في الحلقة.
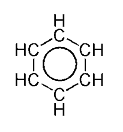
وهذا يقال أنه يحدث بسبب حرية دوران الإلكترونات حول ترتيب دائرى من الذرات, وتتبادل فيما بينها الوضع الأحادي والثنائي للرابطة التساهمية. (لتوضيح أكثر, هذه الروابط يمكن أن تلاحظ كتهجين بين الروابط الأحادية والثنائية, فكل رابطة في الحلقة تكون متطابقة مع الأخرى.) وهذا هو التصور العام للحلقات العطرية الذي تم اقتراحه بواسطة كيكولي. ويتكون هذا التصور للبنزين من شكلان بهما رنين, وهما يمثلان تبادل الوضع للوابط الأحادية والثنائية. ويكون البنزين أكثر ثباتا من "الهيكسا ترايين الحلقي", وهو جزيء نظري.

ويمثل السهم ذو الرأسين هنا عملية الرنين. وهندسيا فإن البنزين شكل سداسي تام. وبصفة عامة فإن الرابطة C=C أقصر من C-C, ولا يجب أن يخلط بين الشكلين حيث أن طول الرابطة C-C يتذبذب.
ويوجد تمثيل أفضل لحلقة البنزين, وهو وضع دائرة حيث تتوزع الكثافة الإلكترونية من الرابطة باي أسفل وأعلى الحلقة. وهذا التمثيل للحلقة أفضل في تمثيل الكثافة الإلكترونية في الحلقة.







